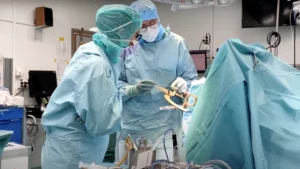
För tio år sedan fick den första patienten i Europa banbrytande immunterapi, så kallade CAR T-celler, på Akademiska sjukhuset i Uppsala. Idag används CAR T-celler som behandling av flera cancersjukdomar såsom lymfom och akut lymfatisk leukemi samt vid återfall av maligna lymfom. Behandlingen har även visat effekt hos patienter med myelom och inflammatoriska sjukdomar såsom SLE och MS där kliniska studier pågår i USA och planeras att starta i Sverige. I veckan uppmärksammades framstegen på ett symposium på Uppsala slott.
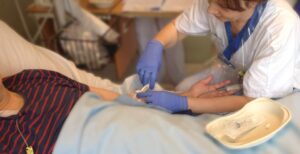
2014 genomfördes den första CAR T-cellsbehandlingen i Europa på Akademiska sjukhuset. Det är en form av immunterapi som alltmer ses som den fjärde hörnstenen i arsenalen av cancerbehandlingar vid sidan av strålning, kirurgi och cytostatika. Foto: Akademiska sjukhuset
– Immunterapi ses alltmer som den fjärde hörnstenen i arsenalen av cancerbehandlingar vid sidan av strålning, kirurgi och cytostatika. CAR T-cellsbehandling är ett exempel och innebär att man förstärker patientens immunförsvar för att döda cancerceller. Specifika immunceller, så kallade T-celler, utrustas med en molekyl som känner igen ett antigen på tumörcellens yta, dvs ett ämne som kroppen uppfattar som främmande, säger Gunilla Enblad, överläkare och professor i onkologi vid Akademiska sjukhuset/Uppsala universitet.

Gunilla Enblad, överläkare och professor i onkologi, Akademiska sjukhuset/Uppsala universitet.
Foto: STAFFAN CLAESSON 20211125
Idag är sex olika CAR T-cellsbehandlingar godkända av de amerikanska och europeiska läkemedelsmyndigheterna FDA och EMA. Tre av dessa är rekommenderade för användning i Sverige av rådet för nya terapier (NT-rådet).
– Mellan 2014 och 2019 fick 39 cancerpatienter CAR T-celler som behandling på Akademiska sjukhuset inom ramen för de första kliniska studierna. Numera är immunterapin godkänd som rutinbehandling vid sidan av andra terapier av flera cancersjukdomar: lymfom, akut lymfatisk leukemi och återfall av maligna lymfom. Terapin har även visat effekt hos patienter med inflammatoriska sjukdomar såsom SLE och MS där kliniska studier pågår i USA och planeras i Sverige. Det är en spännande och dynamisk utveckling vi ser, konstaterar Gunilla Enblad.
Vid CAR T-cellsbehandling renas först T-celler fram från patientens eget blod. I en produktionsanläggning förses de med en ny gen som fungerar som ett slags receptor för tillverkning av ett protein kallat ”chimeric antigen receptor”, CAR. Proteinet innehåller en del av en antikropp och delar av T-cellers naturliga receptor. När behandlingen används vid cancersjukdom gör CAR-proteinet att T-cellerna kan söka upp och döda cancerceller.
För att ge kraft åt utvecklingen av läkemedel för avancerade terapier bildades ATMP-centrum Uppsala hösten 2023. ATMP står för Advanced Therapy Medicinal Products, där ett exempel på den här typen av läkemedel är just CAR T-celler. Läkemedel som ingår är somatiska cellterapier, genterapier, vävnadstekniska produkter och kombinationsläkemedel som innehåller avancerade terapiläkemedel. Bakom satsningen står Akademiska sjukhuset/Region Uppsala och Uppsala universitet. Syftet är framför allt att bidra med stödstrukturer för de forskare som vill utveckla och/eller behandla patienter med läkemedel för avancerad terapi.
FAKTA: CAR T-celler
- CAR T-celler (chimeric antigen receptor T celler) är en immunterapi där patientens egna T-celler utrustas med en CAR-molekyl som känner igen ett antigen på tumörcellens yta.
- Inför behandlingen lämnar patienten ett större blodprov, varifrån T-celler isoleras fram och modifieras med en viral vektor som bär med sig CAR-molekylen. Därefter odlas de modifierade CAR T-cellerna i ett renrum så att de ökar i antal och ges sedan åter till patienten.
- Initialt behandlades primärt lymfom och leukemier, där godkända läkemedel finns idag. I kliniska studier finns CAR T-celler för multipelt myelom, och effekt även hos patienter med inflammatoriska sjukdomar såsom SLE och MS har påvisats. CAR T-celler som känner igen andra tumörer finns också under klinisk utveckling.
Milstolpar för CAR T-cellsbehandling
2010 Första vuxna patienten behandlas i världen vid University of Pennsylvania, USA.
2012 Första barnet i världen behandlas, en då femårig flicka, som svarade bra och fortfarande lever. Familjen har startat The Emily Whitehead Foundation för att stötta cancerforskning.
2013 Science erkände betydelsen av immunterapi med omnämnandet årets genombrott.
13 maj 2014 Första vuxna patienten i Europa behandlades på Akademiska sjukhuset i Uppsala.
2017-2019 CAR T-cellsterapin Kymriah godkänns, som första CAR T-cellsprodukten i världen, i augusti 2017 av FDA, ett år senare aug 2018 av EMA och erhöll rekommendation av NT-rådet (under förfarandet ordnat införande) i maj 2019.
2019 SWECARNET (“Sweden’s CAR T Cell Competence Network”) bildas
2021/2022 Rapporter publiceras om patienter med autoimmuna sjukdomen lupus (SLE) som behandlats med goda resultat med CAR T-celler.
2024 Kliniska studier initierade med CAR T-celler för behandling av SLE respektive MS.
I maj 2024 är sex CAR T-cellsbehandlingar godkända av FDA och EMA; Kymriah, Yescarta, Tecartus, Abecma, Breyanzi och Carvykti. Utav dessa är tre rekommenderade av NT-rådet för användning i Sverige; Kymriah, Yescarta och Tecartus.