Genetisk variation ger ökad känslighet mot cancerläkemedel
Genom att utnyttja cancercellers genetiska variation kan ett redan godkänt läkemedel användas för att mer effektivt slå ut cancerceller hos vissa patientgrupper. Det visar forskare från Uppsala universitet i en ny studie som publicerats i tidskriften eBiomedicine. Resultaten visar på möjligheter till en mer individanpassad och effektivare cancerbehandling.
Människans arvsmassa består av 46 kromosomer, där alla utom x- och y-kromosomerna hos män finns i två uppsättningar. Det gör att personer som har en felaktig gen på den ena kromosomen oftast har en motsvarande fungerande gen på den andra. Men när en tumör bildas kan det bli så att cancercellerna bara har den felaktiga versionen.
– I cancerceller är det vanligt att större eller mindre delar av kromosomerna förloras. Om det då är den felaktiga genen som blir kvar kommer cancercellerna att sakna det protein som genen skulle ha gett upphov till. Det här kallas på engelska Loss of Heterozygosity (LOH) och gör att cancercellerna skiljer sig från de friska cellerna. Det är något som skulle kunna utnyttjas för att utveckla behandlingar som specifikt riktar in sig på cancercellerna, säger Xiaonan Zhang, forskare vid institutionen för immunologi, genetik och patologi och studiens förstaförfattare.

Xiaonan Zhang, forskare vid institutionen för immunologi, genetik och patologi och studiens förstaförfattare.
I den aktuella studien analyserade forskarna ett stort antal gener och hittade en gen som ligger i en dna-region som ofta saknas i cancercellerna i flera sorters cancer. Genen ger upphov till ett enzym i levern som heter CYP2D6. Sedan testade de olika substanser i cancercellmodeller för att se hur substansernas effekt påverkades av CYP2D6-enzymets aktivitet.
– Vi undersökte substanser som ingår i cancerläkemedel som redan används eller som håller på att testas i kliniska prövningar. En av de mest lovande var ett redan godkänt läkemedel som heter talazoparib och som genomgående uppvisade bättre celldödande effekt på levercancerceller om de saknade ett fungerande CYP2D6-enzym, säger Xiaonan Zhang.
Forskarnas opublicerade resultat antyder också att talazoparib kan ha en CYP2D6-beroende effekt i cancerformen neuroblastom och äggstockscancer. De kommer därför att fortsätta att analysera läkemedel som riktar in sig på enzymer vars aktivitet varierar i cancerformer i andra organ.
– Genom att utnyttja LOH och annan naturlig genetisk variation i cancercellerna tror vi att vi kan upptäcka nya behandlingsstrategier som är anpassade specifikt till patientens genetiska profil. Det är en strategi som har förutsättningar att utveckla precisionsmedicinen inte bara vid cancer utan även inom andra sjukdomsområden. Med en behandling som är anpassad till patientens genetiska egenskaper kan effekten förbättras och därmed även sjukdomsutfallet, säger Tobias Sjöblom, professor vid institutionen för immunologi, genetik, som har lett studien.

Tobias Sjöblom, professor vid institutionen för immunologi, genetik, har lett studien.
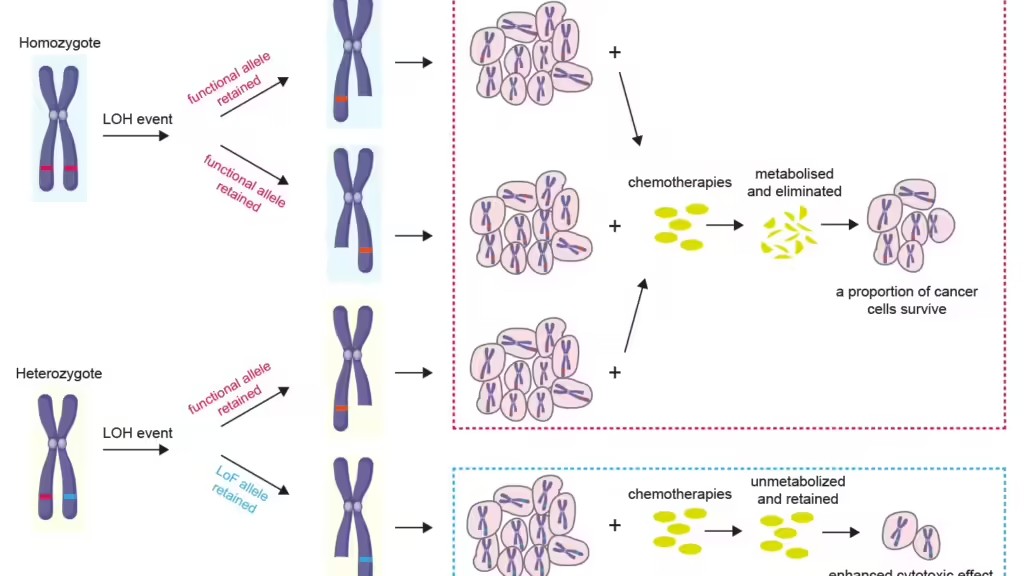
Bilden illustrerar den strategi som används för att identifiera CYP2D6 som ett mål för kollateral dödlighet, vilket drivs av den utbredda förekomsten av förlust av heterozygoti i cancergenom.
Studien gjordes i samarbete med forskare i Schweiz och vid Chemical Biology Consortium Sweden.
Den finansierades av Barncancerfonden, Cancerfonden, Vetenskapsrådet och Erling Perssons stiftelse.
Zhang, Xiaonan et al. (2024), Loss of heterozygosity of CYP2D6 enhances the sensitivity of hepatocellular carcinomas to talazoparib, eBioMedicine, Volume 109, 105368, 10.1016/j.ebiom.2024.105368
https://www.thelancet.com/journals/ebiom/article/PIIS2352-3964(24)00404-3/fulltext